免疫荧光(Immunofluorescence):又称荧光抗体技术,是标记免疫技术中发展最早的一种,根据抗原抗体的特异性结合检测样品中的某种蛋白的方法。
基本原理
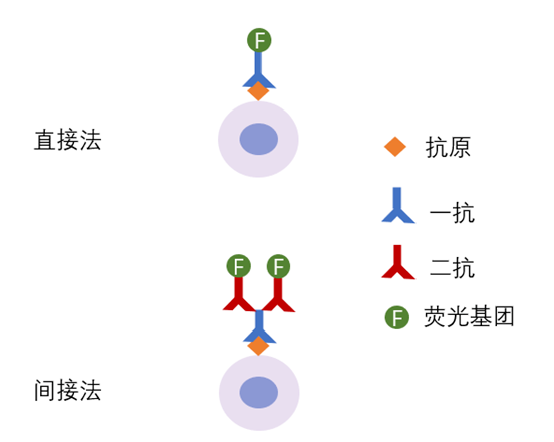
以抗原与抗体反应结合为基础,联合荧光色素标记,对细胞或组织内特定物质进行标记或示踪的一种实验方法。在细胞内形成的抗原抗体复合物上含有标记的荧光素,利用荧光显微镜观察标本,荧光素受外来激发光的照射而发生明亮的荧光,可以看见荧光所在的细胞,从而确定抗原或抗体的性质、定位,以及利用定量技术测定含量。
 IF常规操作步骤(间接法)
IF常规操作步骤(间接法)
1. 固定:根据需要选择适当的固定剂固定细胞,
一般再4%甲醛室温固定15min,1×PBS洗涤3次,每次5min。
2.
通透:使用交联剂固定后的细胞,一般需要再加入抗体孵育前,对细胞进行通透处理,以保证能够达到抗原部位。
选择通透剂应充分考虑抗原蛋白的性质。通透时间一般在5-15min。通透后1×PBS洗涤3次,每次5min。
通常情况下是先固定后通透,但是
如果所检测的抗原是水不溶性的蛋白的话,可以先通透再固定,这样可以通过通透去除许多水溶性的蛋白,从而大大减少了免疫荧光的背景和非特异性信号。
3.
封闭:使用封闭液对细胞进行封闭,室温封闭30min-1h。
一抗结合:吸走封闭液,加入稀释后的一抗,4℃孵育过夜。1×PBS洗涤3次,每次5min。
4.
二抗结合:间接免疫荧光需要使用二抗。室温避光孵育1h。1×PBS洗涤3次,每次5min。
5.
封片及检测:按需求进行核/浆复染,封片,荧光显微镜观察。
 免疫荧光常见问题总结
免疫荧光常见问题总结
1.
信号微弱或没有信号
一般遇到这种情况,可能是实验操作问题,包括实验操作不当、样本保存不当、固定不足、抗体用量不合适、一抗孵育时间不合适、错误的通透方法、二抗使用不当、错误的激发波长等;还有可能是蛋白表达问题,目的蛋白需要诱导表达或者表达量低。
2. 高背景
对于染色过深,遇到这种情况需要我们做的是
优化实验条件,可能是由于封闭不充分、抗体使用浓度过高、抗体孵育时间过长或者孵育温度过高、样本变干、清洗不足、非特异性结合抗体等。
总而言之,要想免疫荧光实验结果尽如人意,首先必须要
做好实验前的准备,了解蛋白详细信息;接着在实验阶段
选择合适的固定剂和通透剂;最后抗体孵育时需摸索出合适的抗体浓度和孵育时间。
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请告知,我们将尽快删除相关内容。




