人体拥有一套复杂且高效的免疫系统,时刻保护着我们免受病毒和细菌的攻击。弱小又无助的原核细胞,经过几亿年的进化,同样演化出了多种防御机制,CRISPR-Cas适应性免疫系统就是其中之一,用于保护它们免受外源DNA和噬菌体的侵染。规律成簇的间隔短回文重复序列(CRISPR)与内切酶Cas9的组合,可以在guide RNA的指引下,靶向并切割入侵者的遗传物质。
研究者们利用这一特点,将CRISPR系统发展成了强大的基因组编辑工具,时至今日,基于CRISPR-Cas的生物学实验技术已经成为基因编辑的主要工具。
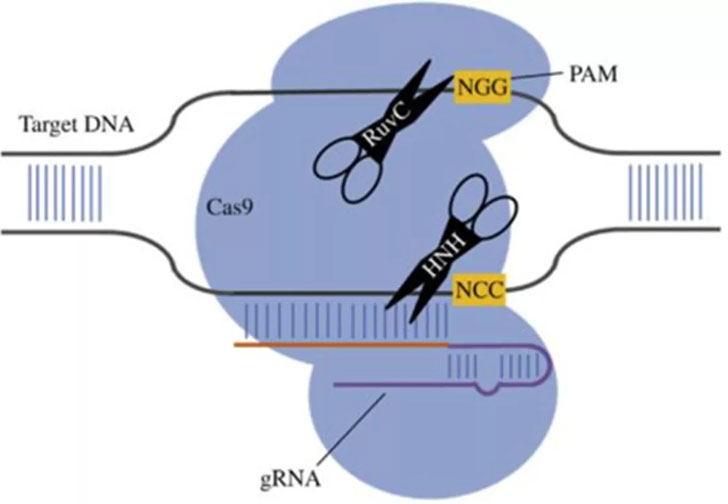
CRISPR-Cas9系统原理示意图
(Wei, et al,Journal of Genetics and Genomics. 2013)
干细胞能够分化成为机体内任何类型的细胞,是研究人体早期发育的理想工具,也是细胞治疗的宝贵资源,但胚胎干细胞的获取,不可避免会严重伤害乃至杀死胚胎,有很大的伦理争议,相关研究在各国都受到严格监管。2006年日本科学家山中伸弥率领的团队在国际顶级期刊上发布了近期的研究成果,将Oct4、Sox2、c-Myc 和 Klf4 四个基因导入小鼠胚胎或皮肤纤维母细胞中,使其重编程而形成类似于胚胎干细胞的细胞类型,并将其命名为诱导多能干细胞(iPS细胞,Induced pluripotent stem cells)。这些细胞在实验室中表现出与胚胎干细胞相似的能力,又避开了胚胎干细胞的伦理问题,这无疑是人类再生医学研究史上的里程碑事件。iPS细胞在疾病模拟、药物筛选和细胞治疗中有着巨大的应用前景,被人们视为细胞疗法的新希望。
基于CRISPR的基因编辑技术和iPS重编程技术一直是近年来的两大热点技术,CRISPR/Cas9已经在多个领域中展现了自己强大的特异性基因靶向能力,被广泛地应用于基因功能发现,蛋白改造,抗体验证,疾病模型构建等领域。而iPS重编程在构建疾病模型和新药开发中有着很高的应用价值。将CRISPR应用到iPS细胞中去,将可能实现个性化的干细胞治疗,造福多种遗传学疾病的患者。那么iPS细胞的基因编辑有哪些成功的应用范例呢?让我们一起来了解一下~
首例CRISPR编辑
干细胞治疗HIV和白血病患者
在人类基因治疗的背景下,基于CRISPR的基因组编辑安全性在很大程度上是未知的。CCR5是对抗人类免疫缺陷病毒1型(HIV-1)感染的一个合理但不是绝对有效的保护性靶点,因为CCR5缺失的血细胞在很大程度上对HIV-1的进入具有抗性。研究者将通过CRISPR编辑的CCR5被敲除的造血干和祖细胞(HSPCs)移植到一位HIV-1感染和急性淋巴母细胞白血病患者体内。急性淋巴细胞白血病在完全供者型细胞嵌合的情况下得到完全缓解(完全缓解:是指所有目标病灶和非目标病灶均消失,且肿瘤标志物正常,是药物或手术等方法治疗疾病评价较好的一级),并且携带CCR5缺失的供者细胞持续超过19个月,没有发生基因编辑相关的不良事件。在抗逆转录病毒治疗中断期间,CD4+细胞中CCR5缺失的百分比略有增加。但研究也表明,虽然成功移植并长期植入了CRISPR编辑的HSPCs,但在淋巴细胞中CCR5缺失的百分比仅为5%左右,这表明该方法还需要进一步优化。但可以预见的是,该临床试验报告将会推动全球范围内基于CRISPR基因编辑手段用于临床治疗,其意义不言而喻。
研究团队也表示,在今后的研究中,将进一步提高基因编辑效率及优化移植方案,有望加速基因编辑造血干细胞移植技术向临床疾病治疗转化的进程。
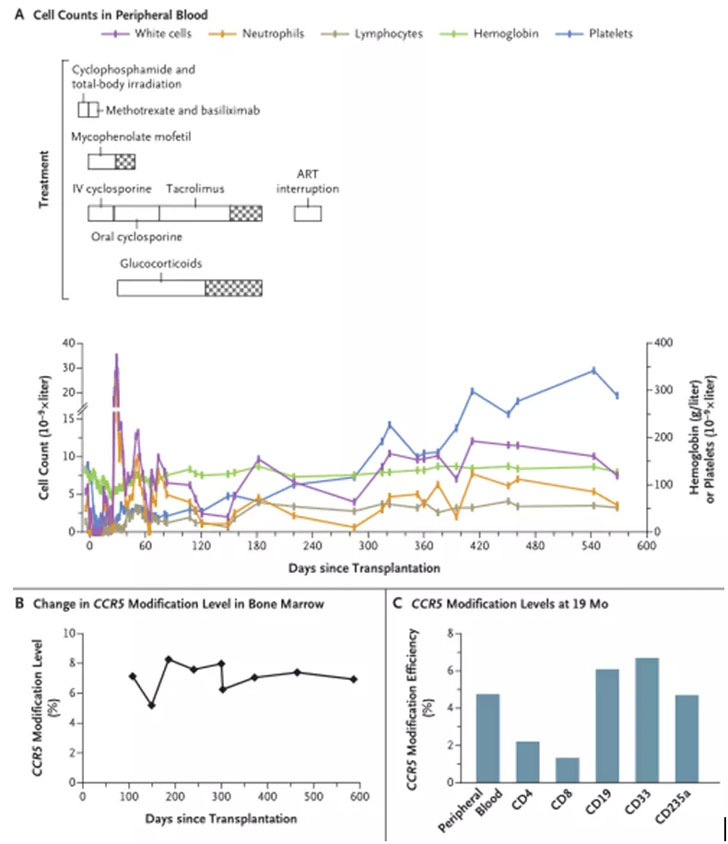
CCR5编辑细胞的植入
(Lei Xu, et al,N Engl J Med. 2019)
结合CRISPR和人类iPSC技术
建立了人类白血病发生模型
人类癌症是通过连续获得体细胞突变而产生连续无性系群体的。人类癌症进化模型可以帮助阐明这一过程,并为早期疾病阶段的治疗干预提供信息,但它们的创建面临着重大挑战。AML是一种血液和骨髓的癌症,骨髓是骨骼内的海绵状组织,血细胞就是在这里产生的。这种疾病主要影响白细胞,是成人最常见的白血病之一。虽然近年来推出了几种针对这种疾病的新药,但都未能显著改变AML患者的治疗效果或生存率。
在此,来自美国纽约州西奈山伊坎医学院肿瘤科学系的Eirini P Papapetrou教授团队,
结合诱导多能干细胞(iPSC)和CRISPR-Cas9技术,建立了急性髓系白血病(AML)克隆进化模型,该模型可以描绘AML从早期到晚期的演变过程。
研究人员通过CRISPR介导的基因编辑引入特定的白血病致病基因突变,改变iPSCs中的DNA序列,从而创建出以一种具有越来越多突变基因的模型,该模型显示出渐进的恶性特征,与人类骨髓疾病中发生的情形相对应,然后利用这些变化的模式能够确定早期疾病阶段的潜在治疗靶标。
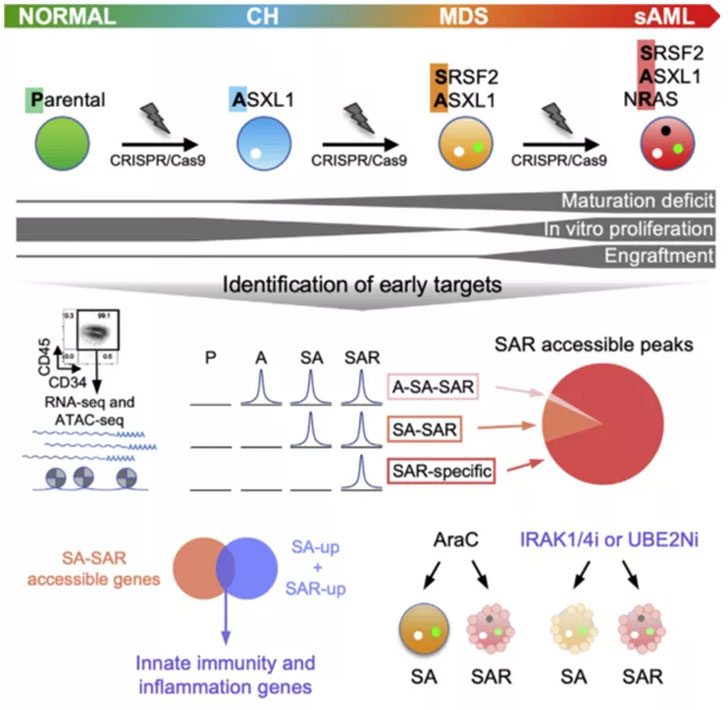
逐步引入人类诱导多能干细胞的驱动突变来模拟白血病发生
(Tiansu Wang, et al,Cell Stem Cell. 2021)
对人iPS细胞进行基因编辑
开发CAR iPS-T细胞疗法
癌症免疫疗法是指利用患者自身的免疫系统来抗击癌症,因对某些癌症惊人的效果而广为人所知。细胞疗法利用从患者肿瘤中获取的免疫细胞,对它们进行加工以增强识别癌细胞能力,然后将其注回患者体内,以达到治疗效果。然而,目前的临床治疗主要是使用患者自身细胞,这种
个性化的患者来源自体T细胞生产方法由于操作复杂、耗时长、成本高,仅限于小规模的临床应用。
来自日本京都大学的Shin Kaneko团队报告了一种对iPS细胞进行基因编辑以产生不依赖患者细胞的通用的癌症免疫疗法。
免疫细胞通过受体对外来细胞表达的蛋白质作出反应,这些外体移植细胞所含蛋白质中重要的是人类白细胞抗原(HLA)。为了规避体外移植的细胞引起的宿主体内免疫反应,使移植细胞能够存活,发现有三种类型的免疫细胞需要被抑制,分别是CD8+ T细胞,CD4+ T细胞和NK细胞,其中CD8+ T细胞引起强烈和危险的反应。一些研究小组已经探索利用基因编辑敲除移植T细胞中的HLA和其他免疫激活蛋白,然而,根据前期的研究报道,这种方法可能会损害T细胞。
iPSC可以为这个问题提供解决方案,iPSC具有无限的扩增潜能,可以分化成任何类型的细胞,包括用于细胞免疫治疗的T细胞。重要的是,
它们的扩增和分化潜能都不受多轮基因编辑的影响。
因此,研究人员探索了需要编辑的基因,分别为CD8+ T细胞选择了B2M,为CD4+ T细胞选择了CITTA,NK细胞选择了一种特殊类型的HLA(HLA-E)此外,
还敲除了PVR基因(编码NK细胞活化受体DNAM-1的配体PVR),这进一步抑制了NK细胞的激活,这些基因之前被认为可以调节各自免疫细胞的活化。
B2M基因敲除的iPS-T细胞可逃避异体CD8 T细胞的反应和裂解
(Bo Wang, et al,Nat Biomed Eng. 2021)
研究者随后将基因编辑过的iPS细胞分化为T细胞(iPS-T细胞),发现iPS-T细胞具有良好的抗癌效果,而不刺激免疫细胞。接着在将利用CAR-T技术将CAR整合到他们的iPS-T细胞中,相比于没有经过基因编辑的CAR-T细胞,经过基因编辑后躲避免疫系统的CAR iPS-T细胞显示出更强的抗癌效果。
经过基因编辑的iPS细胞显示了作为T细胞的通用来源的巨大前景,可能能够用于治疗任何癌症患者。
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请告知,我们将尽快删除相关内容。