腺相关病毒 (Adeno-Associated Virus, AAV) 载体是研究和临床试验中很受欢迎的基因递送载体之一。由于具有低毒性、适合多种组织转导以及基因长期稳定表达的特点,AAV载体极大提高了人体中基因治疗临床试验的安全性和功效性,而这离不开临床级AAV载体的生产和优化。
和其它生物医药制剂的生产一样,用于基因治疗的临床级AAV载体的生产需要严格监测,严格执行质量控制参数,以符合临床安全性和有效性。在AAV载体生产过程中,产品质量同质性、载体纯度和批次一致性是质控的重要方面,除了确保AAV载体的滴度、产量和生物活性外,最重要的是提高AAV载体的纯度。这其中,最
具有挑战的任务是去除掉有缺陷的AAV载体,即去除空的衣壳病毒颗粒或者含有全长基因以外DNA的病毒载体颗粒。
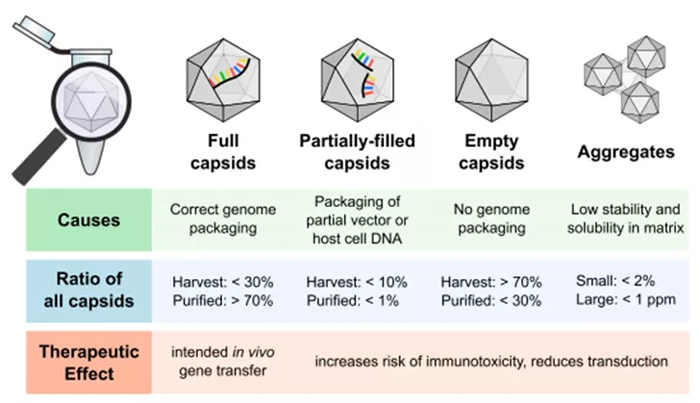
在AAV载体生产过程中,除了产生所需全长目的基因的完整AAV载体,体系中还伴有空衣壳的病毒颗粒、填充了部分基因的病毒颗粒、基因组DNA过度装载的病毒颗粒(图一)、宿主DNA碎片、质粒DNA碎片和核酸酶等杂质的产生。通过GMP级的生产体系优化,尽量降低缺乏目的基因的空壳颗粒、包含片段化或者部分基因组的病毒载体颗粒,以尽可能纯化获得更多高质量的包含完整基因组的病毒载体颗粒。
图一(来源:参考文献7)
在临床级AAV载体的测试和制造过程中,为了保证AAV载体产品在临床转化研究和试验上的功效和安全性,对空衣壳病毒颗粒和完整病毒颗粒的比率进行快速和准确的质控分析显得非常重要。分析AAV载体空壳率的方法有qPCR、ELISA、光密度法、透射电子显微镜法、阴离子交换色谱法和分析型超速离心技术等。下面将依次介绍这几种分析方法的技术特点。
1. qPCR
qPCR是分子生物学实验的常规技术,由于实验简便和特异性,它也广泛用于量化AAV载体基因组的滴度。它通常需要对样本进行化学或酶处理,以消化样本中未包装的DNA以及通过将衣壳蛋白变性以暴露出被包装的基因组DNA。一般来说,qPCR实验对未经纯化或者处理过程中的样本也适合,不影响对AAV载体基因组含量的滴定。
2. ELISA
酶联免疫吸附试验(Enzyme-Linked ImmunoSorbent Assay, ELISA)为免疫学中的经典实验,它通过底物酶促反应显色来测定衣壳蛋白的滴度。首先捕获抗体和AAV载体衣壳蛋白上的抗原构象表位结合在固相载体上,然后通过和检测抗体结合并加入底物实现酶促显色反应。目前rAAV1、rAAV2、rAAV3、rAAV5、rAAV6、rAAV8和rAAV9等血清型抗原表位的特异性单克隆抗体已经商业化应用,这些血清型AAV载体的衣壳蛋白含量相应能进行量化。ELISA法实验步骤繁多,时间周期相对较长,测量结果的可重复性不高。
3. 光密度法
光密度法(Optical Density, OD),也叫紫外线吸收测量法,基于衣壳蛋白血清型和基因组预先确定的消光系数,它通过测量260 nm和280 nm处核酸和蛋白的吸收来定量衣壳蛋白的滴度和AAV载体的含量比。它通常需要用洗涤剂将衣壳蛋白变性以及通过加热来暴露载体基因组。该方法并没有特异于AAV载体测量,其准确度受到样本中残余核酸和蛋白质的影响,因此需要去除样本中其它所有吸收杂质。样本需要进行纯化和浓缩,浓缩样本的浓度要求高于5x10^11 VG/mL,因此该方法比较适合检测分析纯化过的AAV样本。由于OD线性范围小,和qPCR/ELISA的结果验证比较,OD法准确度的重复性不高,其变异系数CV为15%。OD法实验操作简便,仪器简单,从方法学上它本质是一个检测器,可以方便整合到阴离子交换色谱技术或者分析型超速离心技术中。
4. 透射电子显微镜法(Transmission Electron Microscopy, TEM)
透射电子显微镜是测量AAV空衣壳相对数量的直接工具,也是常用的半定量测量方法。透射电子显微镜使用加速电子束穿过待检测样品,形成了纳米级别分辨率的图像。它通常使用负染色,通过重金属染色剂甲酸铀酰增加对比度,负染色后背景是暗的,所观察对象AAV载体是亮的。在比例尺为100 nm的透射电子图像上可以观察到直径约为25nm的AAV载体颗粒。由于甲酸铀酰染色剂能穿透AAV空衣壳颗粒,使其看起来像有一个中心黑暗点的亮环。包含完整基因组的病毒颗粒由于衣壳中封装了DNA,从空间上阻止甲酸铀酰染料的进入,整个衣壳蛋白不含染料未形成染色,呈现出中心明亮的颗粒状病毒。填充了部分基因组的衣壳,其衣壳中心稍微偏暗一些(图二)。负染色后通过透射电子显微镜观察,空壳病毒颗粒和包含基因组的实心病毒颗粒很容易得到区分。
图二(来源:参考文献4)
空壳-完整衣壳比率的量化取决于透射电镜的图像分析,这对获得准确结果提出了若干挑战。为了分析空壳率,必须为每个AAV样品拍摄多张图像,每张图像的衣壳颗粒含量变化一般不超过2%,需要对数千个衣壳颗粒进行成像和分析,以确保统计学的显著性。由于图像背景噪声和图像识别度的差异,这给图像分析增加了很大难度。且对于非纯化样品,由于细胞裂解物中存在的蛋白质和细胞碎片会干扰电镜图像中AAV衣壳颗粒的准确鉴定。
5. 阴离子交换色谱法(Anion-Exchange Chromatography, AEC)
阴离子交换色谱法(Anion-Exchange Chromatography,AEC)适用于多种血清型的空衣壳颗粒和完整衣壳颗粒的分离,是AAV载体下游生产工艺中广泛使用的纯化方式。由于不同血清型的衣壳颗粒所带的负电荷,与其封装了完整基因组DNA后的病毒颗粒所带的负电荷有差异,导致不同的衣壳病毒颗粒之间,它们的等电点存在差异。基于这一差异,AEC通过正电荷固定相分离待检测的样品。目前AEC的分析方法可以分离AAV1, AAV2, AAV5, AAV6, AAV8和AAV9等几种血清型的空壳颗粒和实心颗粒。
该方法检测的样本浓度范围取决于检测器的灵敏度。通过与TEM和AUC等方法的比较,AEC的准确度得到了验证,使用紫外线检测器,AEC方法显示出高重复性(变异系数CV<1%-4%)和中等精度(变异系数CV为2%-5%)。紫外线检测器能检测到的样本浓度下限约为1x10^11 VG/mL。通过结合高效液相色谱HPLC,可以量化洗脱液中空壳颗粒和实心颗粒的含量比,空壳颗粒和实心颗粒之间的充分分离需要开发和优化每种血清型的流动相条件。不过目前空壳颗粒、部分完整衣壳颗粒和实心颗粒的基线分离仍未有效解决。简而言之,阴离子交换色谱法的分辨率有待提高,且不同血清型的病毒颗粒的空壳率表征需要摸索不同的流动相条件,需要建立不同的分析方法。
6. 分析型超速离心技术(Analytical UltraCentrifugation, AUC)
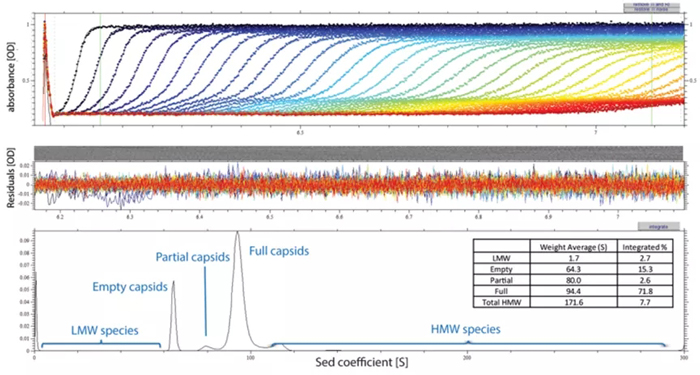
分析型超速离心技术(Analytical Ultracentrifugation, AUC)已广泛用于AAV载体颗粒的表征和生产过程中的定量,它能准确表征样本中各个组分的异质性、聚集体、空壳颗粒、包装部分基因组的颗粒和包装完整基因组的实心颗粒,测定它们之间的相对含量极大提高了分辨率。在离心过程中,沉降速度(Sedimentation-Velocity, SV)与样本中各个组分的分子量和颗粒大小的分布相关联。包装了完整基因组DNA的实心病毒颗粒和包装了部分基因组的颗粒的沉降速度大于空心病毒颗粒的沉降速度。通过紫外线吸收或者Raleigh干扰,AUC实时扫描离心过程中样本中各个组分随着时间其沉降剖面分布状态的变化过程,根据分子量大小和扩散系数计算出各个组分的沉降系数。基于空壳病毒颗粒和实心病毒颗粒沉降系数的不同,准确测定出空壳病毒颗粒的含量、包装完整基因组的实心病毒颗粒和包装部分基因组颗粒的含量(图三),同时还能检测样本中的其它产物如病毒颗粒聚集体、病毒载体碎片和基因组碎片等的相对含量。
图三(来源:参考文献4)
AUC在定量含量比方面具有两个优点:首先它具有高度可重复性,其变异系数CV仅为2%;其二它能很好从空壳病毒颗粒和实心病毒颗粒中区分出包装了部分基因组的病毒颗粒,这是其它很多分析方法所达不到的分辨率。尽管分析功能强大,SV-AUC技术分析时通常需要样本浓度高达5x10^12 VG/mL,需要样本量500uL左右,这可能会影响到生产效率和工艺放大。AUC每次运行的时间约为6个小时,一次运行可分析3-7个样本,通量相对有限。一般来说,当样本中聚集体的含量低于3%-5%时,AUC不适合对聚集体进行定量,此时AUC系统的重复性和准确度会受到很大的偏差影响。
AUC技术将超速离心机和光学检测系统相结合,直接检测分析样本中AAV载体颗粒的特性,有助于AAV载体的质量控制和确保不同批次的临床级AAV载体产品保持一致性。
空壳率分析方法总结
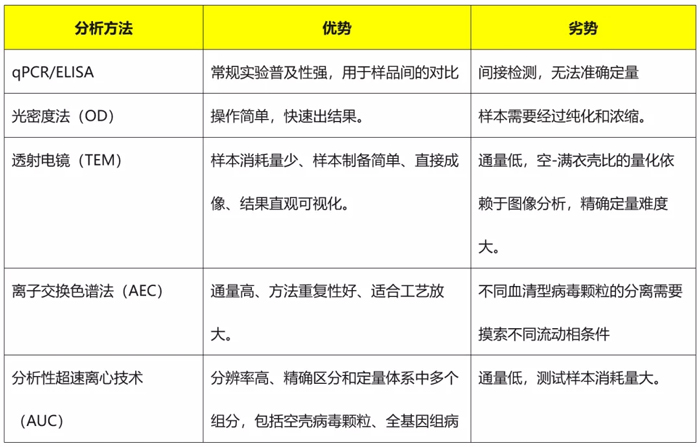
表一:各个分析方法的技术特点
小结:
这篇文章主要介绍了在临床级AAV载体的生产过程中,AAV载体病毒颗粒的纯化以及表征空壳率所用到的多种分析方法。每种分析方法有一定的适用性,除了上述的分析方法,其它的一些分析方法如毛细管等电聚焦技术和电荷检测质谱法也在发展中,目的都是为了更好地表征AAV载体的纯度、均一性和批次一致性等。可以发现,分析型超速离心技术虽然通量不高,但能实现对病毒颗粒产物特性的高分辨率和定量分析。在生产纯化过程中根据需要不断优化组合多种技术分析和去除杂质,产生较安全更高质量的临床级AAV载体产品,以更好满足临床试验的需求。
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请告知,我们将尽快删除相关内容。